Autor:
Bobbie Johnson
Datum Stvaranja:
10 Travanj 2021
Datum Ažuriranja:
1 Srpanj 2024

Sadržaj
Postupak cijepanja vode (H2O) u svoje sastavne dijelove (vodik i kisik) pomoću električne energije naziva se elektroliza. Plinovi dobiveni elektrolizom mogu se sami koristiti - na primjer, vodik služi kao jedan od najčišćih izvora energije. Iako naziv ovog procesa može zvučati pomalo pametno, zapravo je lakše nego što se može činiti ako imate odgovarajuću opremu, znanje i malo iskustva.
Koraci
1. dio od 2: Pripremite opremu
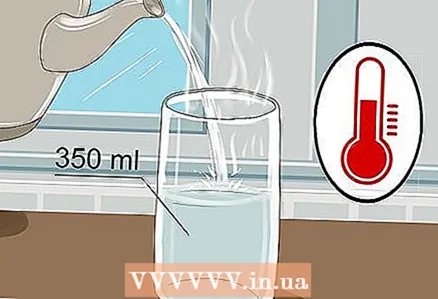 1 Uzmite čašu od 350 ml i ulijte toplu vodu u nju. Nema potrebe puniti čašu do vrha, dovoljno je samo malo vode. Hladna voda će poslužiti, iako topla voda bolje provodi struju.
1 Uzmite čašu od 350 ml i ulijte toplu vodu u nju. Nema potrebe puniti čašu do vrha, dovoljno je samo malo vode. Hladna voda će poslužiti, iako topla voda bolje provodi struju. - Voda iz slavine i flaširana voda će biti dovoljni.
- Topla voda ima manji viskozitet, što olakšava kretanje iona.
 2 Otopite 1 žlicu (20 grama) kuhinjske soli u vodi. U čašu ulijte sol i promiješajte vodu da se otopi. To će stvoriti slanu otopinu.
2 Otopite 1 žlicu (20 grama) kuhinjske soli u vodi. U čašu ulijte sol i promiješajte vodu da se otopi. To će stvoriti slanu otopinu. - Natrijev klorid (tj. Kuhinjska sol) je elektrolit koji povećava električnu vodljivost vode. Sama po sebi, voda ne provodi dobro struju.
- Nakon što povećate električnu vodljivost vode, struja koju stvara baterija lakše će proći kroz otopinu i učinkovitije razgraditi molekule na vodik i kisik.
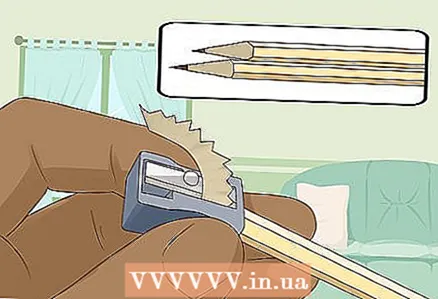 3 Naoštrite dvije tvrde meke olovke na oba kraja kako biste otkrili olovo. Ne zaboravite ukloniti gumicu s olovaka. Grafitna šipka trebala bi stršiti s oba kraja.
3 Naoštrite dvije tvrde meke olovke na oba kraja kako biste otkrili olovo. Ne zaboravite ukloniti gumicu s olovaka. Grafitna šipka trebala bi stršiti s oba kraja. - Grafitne šipke poslužit će kao izolirane elektrode na koje priključujete bateriju.
- Grafit je dobro prilagođen za ovaj eksperiment jer se ne otapa niti korodira u vodi.
 4 Izrežite list kartona dovoljno velik da ga položite na staklo. Upotrijebite prilično debeli komad kartona koji neće popustiti nakon što u njemu izbušite dvije rupe. Izrežite kvadratni komad iz kutije za cipele ili slično.
4 Izrežite list kartona dovoljno velik da ga položite na staklo. Upotrijebite prilično debeli komad kartona koji neće popustiti nakon što u njemu izbušite dvije rupe. Izrežite kvadratni komad iz kutije za cipele ili slično. - Karton se koristi za držanje olovaka u vodi tako da ne dodiruju stranice i dno stakla.
- Karton je neprovodljiv pa ga možete sigurno staviti na staklo.
 5 Olovkama izbušite dvije rupe u kartonu. Karton probušite olovkama - u tom će slučaju biti čvrsto stegnute i neće kliziti. Pazite da grafit ne dodiruje stranice ili dno stakla, inače će ometati pokus.
5 Olovkama izbušite dvije rupe u kartonu. Karton probušite olovkama - u tom će slučaju biti čvrsto stegnute i neće kliziti. Pazite da grafit ne dodiruje stranice ili dno stakla, inače će ometati pokus.
2. dio od 2: Provedite pokus
 1 Spojite jednu žicu s aligatorskim kopčama na svaki priključak baterije. Baterija će poslužiti kao izvor električne struje, a kroz žice sa stezaljkama i grafitnim šipkama struja će doprijeti do vode.Spojite jednu žicu sa stezaljkom na pozitivnu, a drugu na negativni pol baterije.
1 Spojite jednu žicu s aligatorskim kopčama na svaki priključak baterije. Baterija će poslužiti kao izvor električne struje, a kroz žice sa stezaljkama i grafitnim šipkama struja će doprijeti do vode.Spojite jednu žicu sa stezaljkom na pozitivnu, a drugu na negativni pol baterije. - Koristite bateriju od 6 volti. Ako ga nemate, umjesto njega možete koristiti 9-voltnu bateriju.
- Odgovarajuću bateriju možete nabaviti u trgovini električnom energijom ili supermarketu.
 2 Spojite druge krajeve žica s olovkama. Čvrsto pričvrstite stezaljke od metalne žice na grafitne šipke. Možda ćete morati oljuštiti još malo drva s olovaka kako kvačice ne bi skliznule s grafitnih šipki.
2 Spojite druge krajeve žica s olovkama. Čvrsto pričvrstite stezaljke od metalne žice na grafitne šipke. Možda ćete morati oljuštiti još malo drva s olovaka kako kvačice ne bi skliznule s grafitnih šipki. - Tako ćete zatvoriti krug, a struja iz baterije teći će kroz vodu.
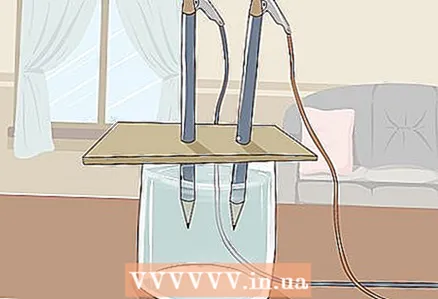 3 Karton stavite na staklo tako da slobodni krajevi olovaka budu potopljeni u vodu. List kartona trebao bi biti dovoljno velik da stane na staklo. Pazite da ne ometate pravilan položaj olovaka.
3 Karton stavite na staklo tako da slobodni krajevi olovaka budu potopljeni u vodu. List kartona trebao bi biti dovoljno velik da stane na staklo. Pazite da ne ometate pravilan položaj olovaka. - Da bi pokus bio uspješan, grafit ne smije dodirivati stijenke i dno stakla. Ponovno provjerite ovo i po potrebi namjestite olovke.
 4 Gledajte kako se voda dijeli na vodik i kisik. Mjehurići plina počet će se dizati iz grafitnih šipki uronjenih u vodu. To su vodik i kisik. Vodik će se oslobađati na negativnom polu, a kisik na pozitivnom polu.
4 Gledajte kako se voda dijeli na vodik i kisik. Mjehurići plina počet će se dizati iz grafitnih šipki uronjenih u vodu. To su vodik i kisik. Vodik će se oslobađati na negativnom polu, a kisik na pozitivnom polu. - Čim spojite žice na bateriju i grafitne šipke, električna će struja teći kroz vodu.
- Na olovci koja je povezana s negativnim polom formirat će se više mjehurića plina, jer se svaka molekula vode sastoji od dva atoma vodika i jednog atoma kisika.
Savjeti
- Ako nemate olovke s grafitnim vratilom, umjesto njih možete upotrijebiti dvije male žice. Samo omotajte jedan kraj svake žice oko odgovarajućeg pola baterije, a drugi umočite u vodu. Rezultat će biti isti kao i kod olovaka.
- Pokušajte koristiti drugu bateriju. Količina struje ovisi o naponu baterije, što pak utječe na brzinu cijepanja molekula vode.
Upozorenja
- Ako u vodu dodate elektrolit, poput soli, imajte na umu da će eksperiment generirati malu količinu nusproizvoda poput klora. U tako malim količinama je siguran, ali možete osjetiti blagi miris klora.
- Izvedite ovaj eksperiment pod nadzorom odrasle osobe. Povezan je s električnom energijom i plinovima te stoga može biti opasan, iako malo vjerojatan.
Što trebaš
- Dvije tvrdo-meke olovke
- Jedna baterija od 6 ili 9 volti
- Staklo zapremine 350 mililitara
- 2 žice s krokodilskim kopčama
- Oštrač za olovke
- Sol