Autor:
Christy White
Datum Stvaranja:
8 Svibanj 2021
Datum Ažuriranja:
1 Srpanj 2024

Sadržaj
- Kročiti
- Metoda 1 od 3: Prvi dio: Razumijevanje elektronskih ljuski
- Metoda 2 od 3: Drugi dio: Pronalaženje valentnih elektrona u metalima, osim prijelaznih metala
- Metoda 3 od 3: Treći dio: Pronalaženje valentnih elektrona u prijelaznim metalima
- Savjeti
- Potrebe
Valentni elektroni leže u vanjskoj ovojnici elementa. Broj valentnih elektrona u atomu određuje vrstu kemijske veze koju ovaj element može stvoriti. Najbolji način da saznate broj valentnih elektrona je upotreba periodnog sustava elemenata.
Kročiti
Metoda 1 od 3: Prvi dio: Razumijevanje elektronskih ljuski
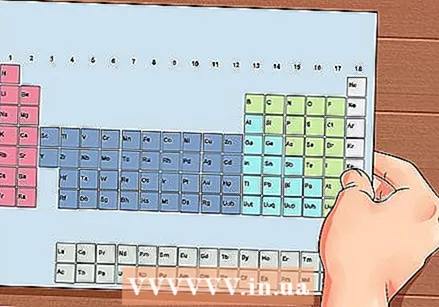 Periodni sustav elemenata. Ovo je tablica s kodovima boja, gdje se u svakoj ćeliji prikazuje element s atomskim brojem i 1 do 3 slova kao simbolom.
Periodni sustav elemenata. Ovo je tablica s kodovima boja, gdje se u svakoj ćeliji prikazuje element s atomskim brojem i 1 do 3 slova kao simbolom. 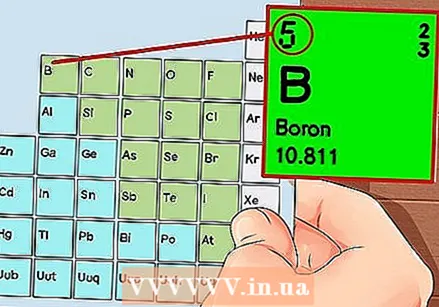 Pronađite atomski broj elementa. Atomski broj nalazi se iznad ili pored simbola elementa. Na primjer: Bor (B) ima atomski broj 5, što znači da ima 5 protona i 5 elektrona.
Pronađite atomski broj elementa. Atomski broj nalazi se iznad ili pored simbola elementa. Na primjer: Bor (B) ima atomski broj 5, što znači da ima 5 protona i 5 elektrona. 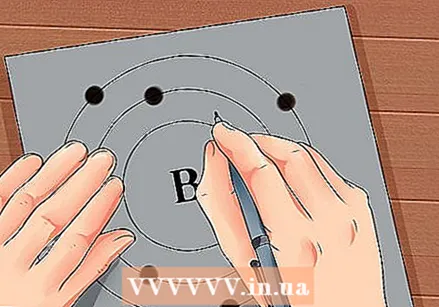 Nacrtajte jednostavan prikaz atoma i smjestite elektrone u orbitu oko jezgre. Ti se poslovi nazivaju i ljušture ili razine energije. Maksimalni broj elektrona koji može biti u istoj ljusci je fiksiran, a ljuske se pune iz unutarnje u vanjsku orbitu.
Nacrtajte jednostavan prikaz atoma i smjestite elektrone u orbitu oko jezgre. Ti se poslovi nazivaju i ljušture ili razine energije. Maksimalni broj elektrona koji može biti u istoj ljusci je fiksiran, a ljuske se pune iz unutarnje u vanjsku orbitu. - K Ljuska (unutarnja): najviše 2 elektrona.
- L ljuska: najviše 8 elektrona.
- M ljuska: najviše 18 elektrona.
- N Školjka: maksimum 32 elektrona.
- O ljuska: maksimum 50 elektrona.
- P Ljuska (vanjska): maksimalno 72 elektrona.
 Pronađite broj elektrona u vanjskoj ljusci. To su valentni elektroni.
Pronađite broj elektrona u vanjskoj ljusci. To su valentni elektroni. - Kad je valentna ljuska puna, element je stabilan.
- Ako valentna ljuska nije puna, tada je element reaktivan, što znači da se može kemijski povezati s atomom drugog elementa. Svaki atom dijeli svoje valentne elektrone u pokušaju da valentnu ljusku napuni.
Metoda 2 od 3: Drugi dio: Pronalaženje valentnih elektrona u metalima, osim prijelaznih metala
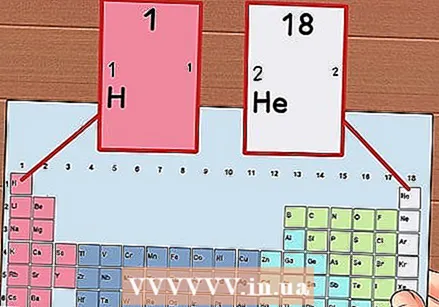 Označite svaki stupac periodnog sustava brojevima od 1 do 18. Vodik (H) je na vrhu stupca 1, a helij (He) na vrhu stupca 18. To su različite skupine elemenata.
Označite svaki stupac periodnog sustava brojevima od 1 do 18. Vodik (H) je na vrhu stupca 1, a helij (He) na vrhu stupca 18. To su različite skupine elemenata. 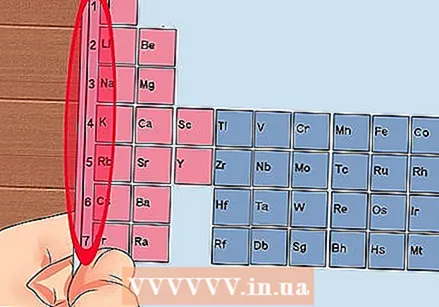 Dajte svakom retku broj, od 1 do 7. To su razdoblja elemenata i odgovaraju broju ljuski ili energetskim razinama atoma.
Dajte svakom retku broj, od 1 do 7. To su razdoblja elemenata i odgovaraju broju ljuski ili energetskim razinama atoma. - Vodik (H) i helij (He) imaju po jednu ljusku, dok Francij (Fr) ima 7.
- Lantanidi i aktinidi su grupirani i navedeni ispod glavne tablice. Svi lantanidi pripadaju razdoblju 6, skupini 3, a svi aktinidi pripadaju razdoblju 7, skupini 3.
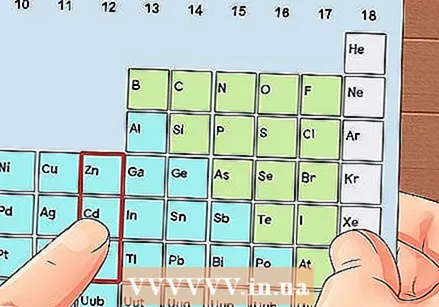 Pronađite element koji nije prijelazni metal. Prijelazni metali su u skupinama od 3 do 12. Brojevi skupina ostalih metala označavaju broj valentnih elektrona.
Pronađite element koji nije prijelazni metal. Prijelazni metali su u skupinama od 3 do 12. Brojevi skupina ostalih metala označavaju broj valentnih elektrona. - Skupina 1: 1 valentni elektron
- Skupina 2: 2 valentna elektrona
- Skupina 13: 3 valentna elektrona
- Skupina 14: 4 valentna elektrona
- Skupina 15: 5 valentnih elektrona
- Skupina 16: 6 valentnih elektrona
- Skupina 17: 7 valentnih elektrona
- Skupina 18: 8 valentnih elektrona - osim helija koji ima 2
Metoda 3 od 3: Treći dio: Pronalaženje valentnih elektrona u prijelaznim metalima
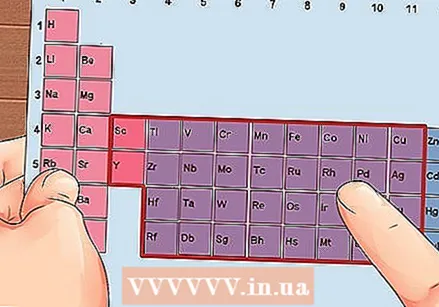 Pronađite element iz skupina 3 do 12, prijelazni metali.
Pronađite element iz skupina 3 do 12, prijelazni metali. Odredite broj valentnih elektrona na temelju broja grupe. Ti brojevi grupa odgovaraju mogućem broju valentnih elektrona.
Odredite broj valentnih elektrona na temelju broja grupe. Ti brojevi grupa odgovaraju mogućem broju valentnih elektrona. - Skupina 3: 3 valentna elektrona
- Skupina 4: 2 do 4 valentna elektrona
- Skupina 5: 2 do 5 valentnih elektrona
- Skupina 6: 2 do 6 valentnih elektrona
- Skupina 7: 2 do 7 valentnih elektrona
- Skupina 8: 2 ili 3 valentna elektrona
- Skupina 9: 2 ili 3 valentna elektrona
- Skupina 10: 2 ili 3 valentna elektrona
- Skupina 11: 1 ili 2 valentna elektrona
- Skupina 12: 2 valentna elektrona
Savjeti
- Prijelazni metali mogu imati valentne ljuske koje nisu u potpunosti pune. Određivanje točnog broja valentnih elektrona u prijelaznim metalima zahtijeva određene principe kvantne teorije koji su izvan dosega ovog rada.
Potrebe
- Periodni sustav elemenata
- Olovka
- Papir